申请提交后,我们将在24小时内联系您。
请放心填写您的个人信息,该信息仅用于“摩熵医药企业版”的试用申请。
提交申请即默认注册摩熵医药企业版账号,申请通过后可使用此手机号登录试用。
购买咨询:400-9696-311转1
申请提交后,我们将在24小时内联系您。
请放心填写您的个人信息,该信息仅用于“摩熵医药企业版”的试用申请。
提交申请即默认注册摩熵医药企业版账号,申请通过后可使用此手机号登录试用。
购买咨询:400-9696-311转1
您的试用申请已提交,我们将在24小时内与您联系
您的试用申请已提交,我们将在24小时内与您联系


7天免费试用

7天免费试用

本文目录:
一、数据库价值&特色
1. 数据库简介
2. 数据库价值
3. 受众人群
二、数据库入口
1. 数据库入口
2. 申请试用入口
三、使用场景示例
1. 查询“阿莫西林胶囊”的详细临床试验数据
2. 查看2024年百济神州登记的国际多中心试验情况
3. 查询登记号CTR20221196的临床试验详情
四、联系我们
----------------------------------------------------------------------------------------------------------------------
一、数据库价值&特色
1. 数据库简介
中国临床试验数据库收录了药品审评中心(CDE)和中国临床试验注册中心两大平台登记的所有临床试验详细信息。具体内容涵盖临床试验基本信息、临床试验设计、患者招募信息、研究者信息、药物信息、适应症、临床研发阶段、临床试验状态以及临床试验结果等信息。该库旨在监测获批临床药物的研发进度及最新动态,同时可为企业在研发立项或购买新产品提供决策依据。
数据库的检索字段有试验题目、登记号、药品名称、剂型、靶点、适应症、申办单位、临床机构、对照药等;也支持条件筛选,筛选项有数据来源、试验范围、试验状态、试验分期、药品类型、试验分类等。
其中,订阅功能可以对登记号、品种、申办单位进行一键订阅,实现多条相关信息合并接收,更便捷地实时查看临床试验最新动态,监测获批临床药物的临床试验进度;
数据对比功能,可以更加直观地比较不同临床试验信息,如入选/排除标准、试验药及用法用量、终点指标、入组人数、临床时间轴等信息,降低临床试验研究的时间成本,提高工作效率。
2. 数据库价值
· 帮助用户溯源临床试验进度、跟踪竞品进程试验信息
· 快速检索目标靶点、成分、适应症的临床实验开展情况
· 监测获批临床药物的研发进度及最新动态,为企业研发立项或购买新品提供决策依据
· 查询主要临床与参与临床机构,为药企提供药物临床机构信息,助力药物临床三期研发
3. 受众人群
药物立项、医药投资、市场调研、商务拓展团队、战略研究部、医疗机构、在校师生等。
二、数据库入口
1.数据库入口
操作路径:
数据库首页中部左侧/顶部菜单栏选择【药品研发】数据库群中的【中国临床试验】数据库,然后点击进入
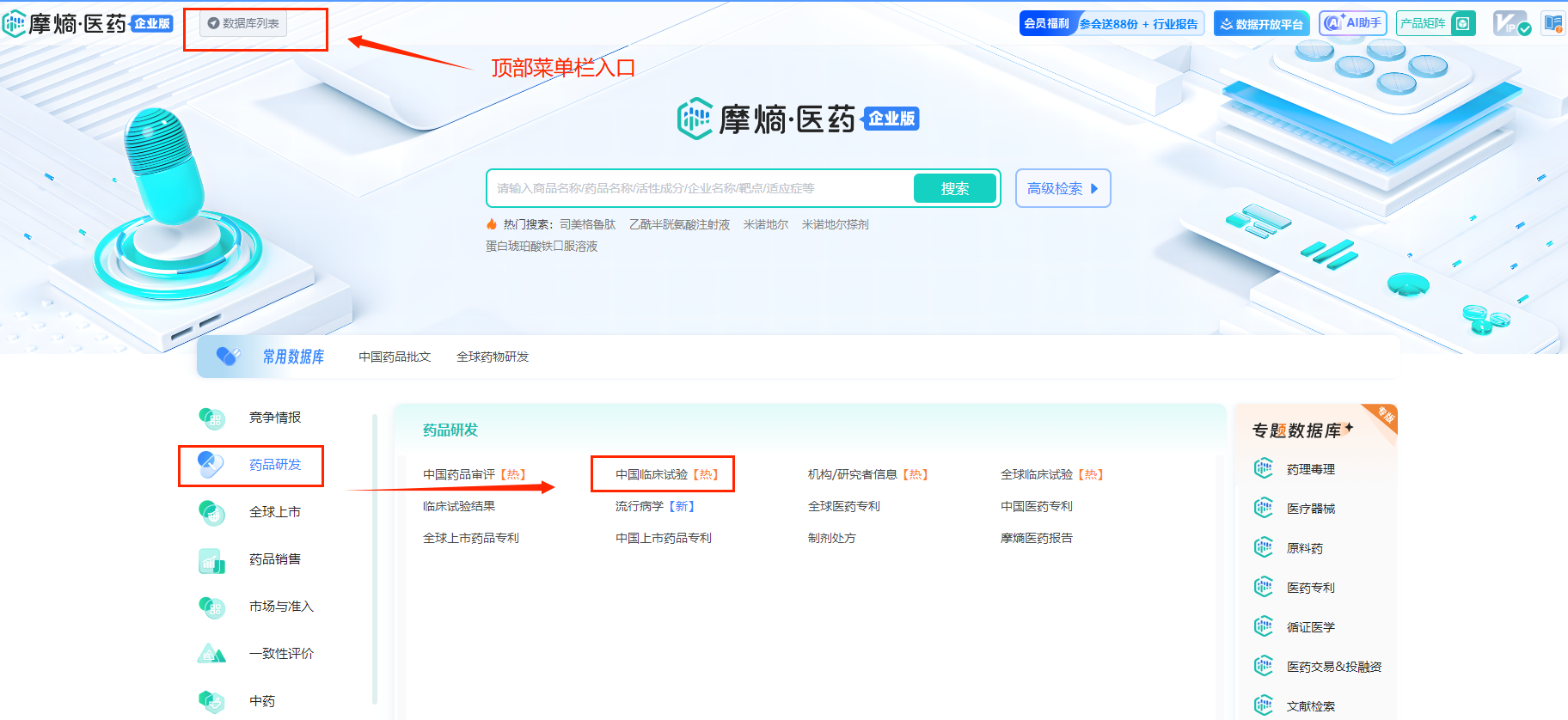
2.申请试用入口
https://vip.pharnexcloud.com/solution/clinical?auto=1
三、使用场景示例
1. 查询“阿莫西林胶囊”的详细临床试验数据
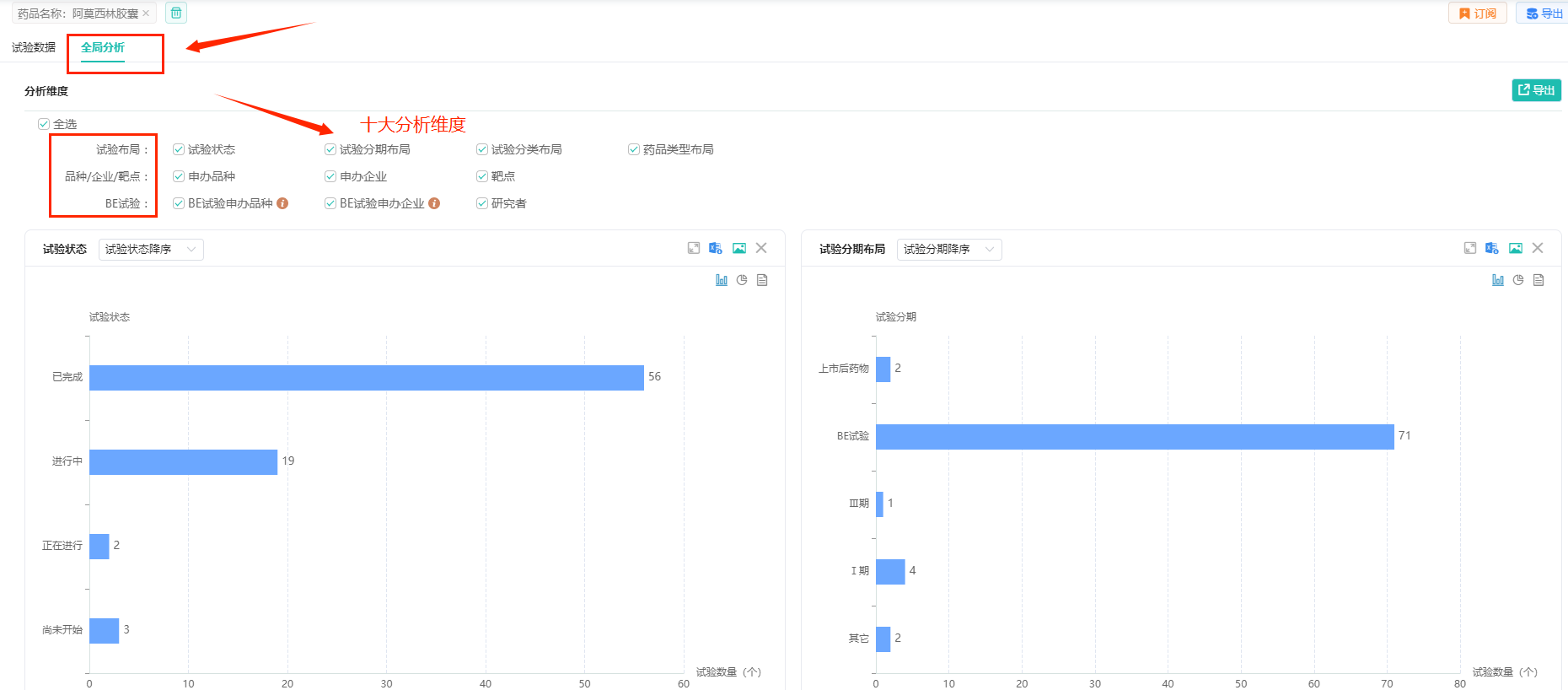
操作路径:【药物名称】输入【阿莫西林胶囊】,点击搜索按钮后,即可查询到本药品的详细展示的临床试验数据(如下图所示),并按照自己的需求切换四种不同维度数据(按登记号浏览、按品种浏览、按申办单位浏览、按临床机构浏览)进行查看。
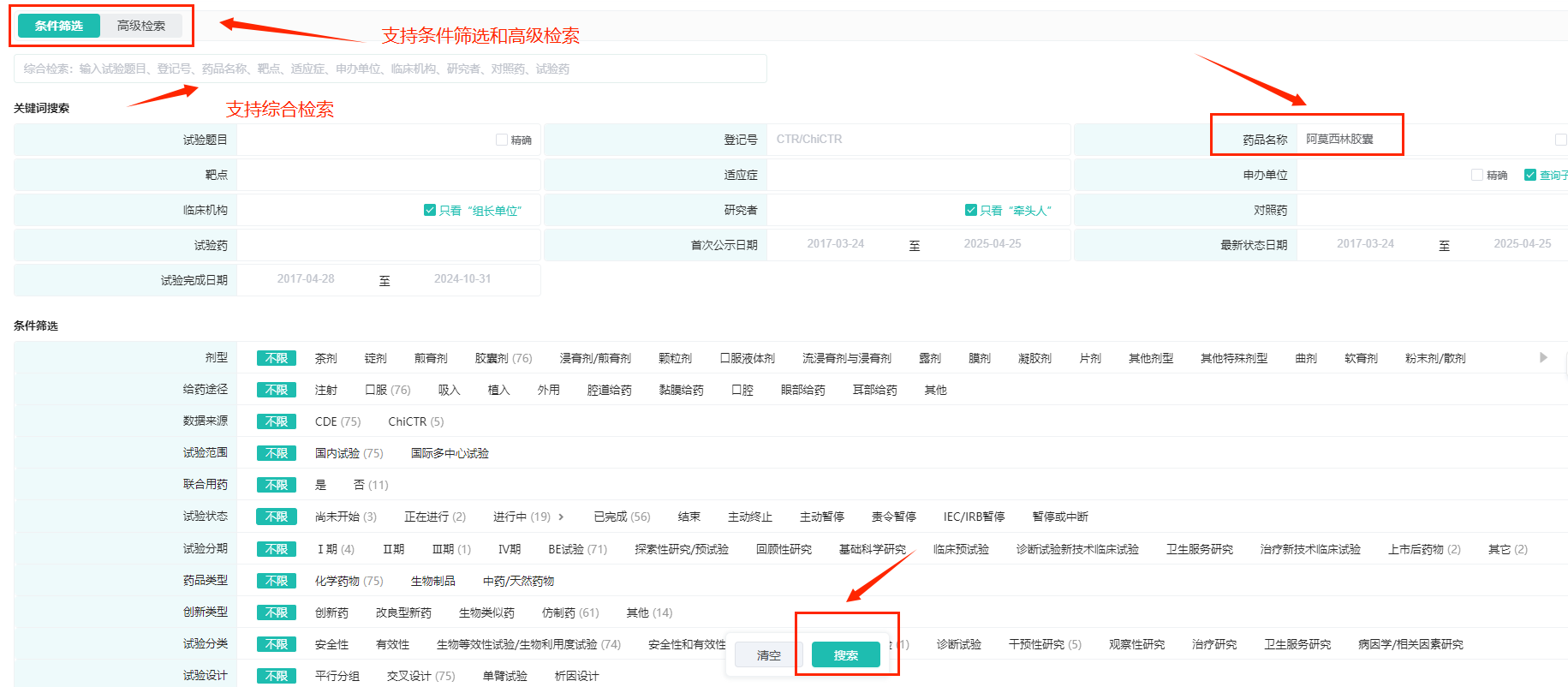
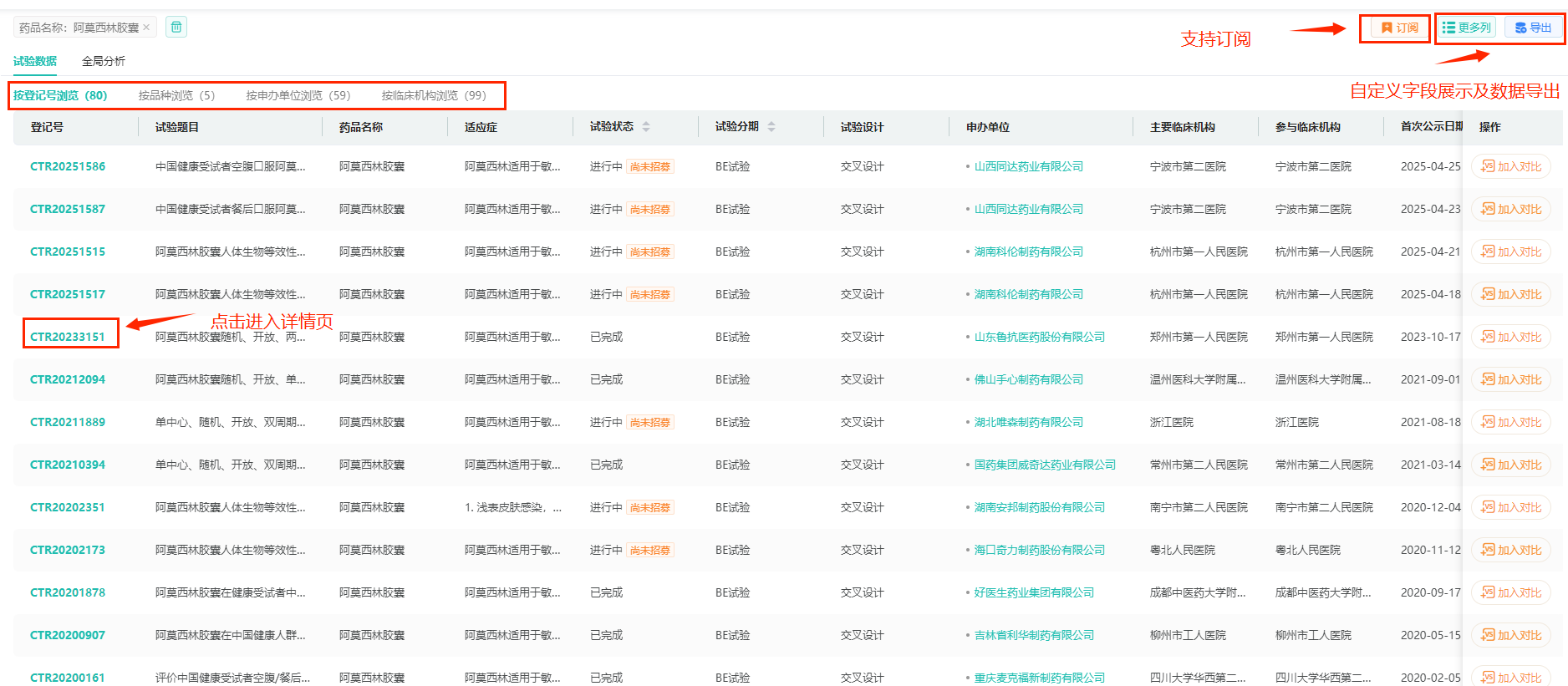
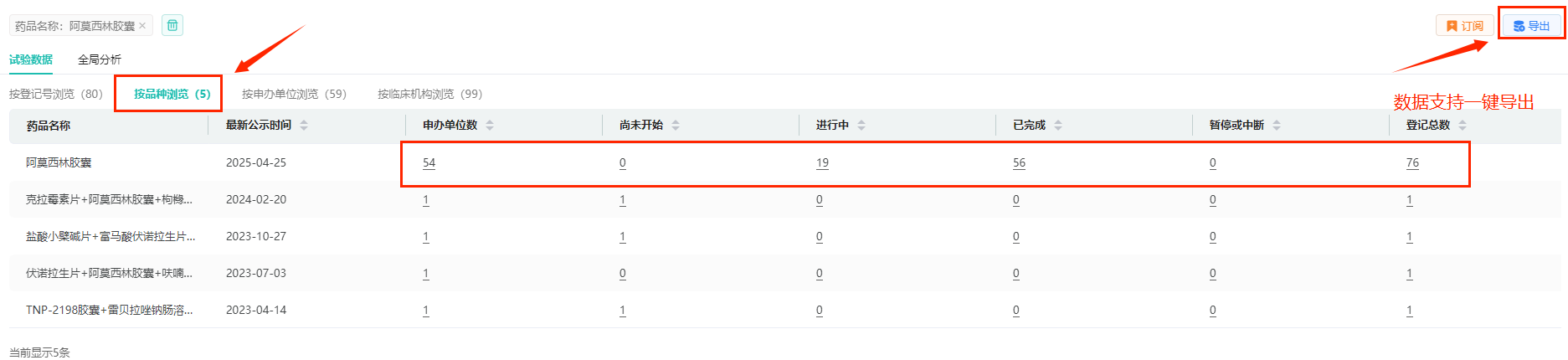
按品种浏览,可以看到阿莫西林胶囊的临床试验登记总数有76个,涉及申办单位数54家,临床试验处于进行中的有19个,已完成的有56个。
点击【全局分析】,可以对阿莫西林胶囊在中国的临床试验进行整体分析,包括“试验状态、试验分期布局、试验分类布局、药品类型布局、申办品种、申办企业、靶点、BE试验申办品种、BE试验申办企业、研究者”等多个维度的数据进行详细分析,并且每个分析版块都可单独保存下载,对于需要进行临床分析报告写作的用户而言,可以节省制作分析图的时间。
在BE试验申办企业分析维度中,可以看到阿莫西林胶囊BE试验申办企业TOP10/TOP50分布情况,支持数量降序/升序展示,也支持一键导出列表数据。
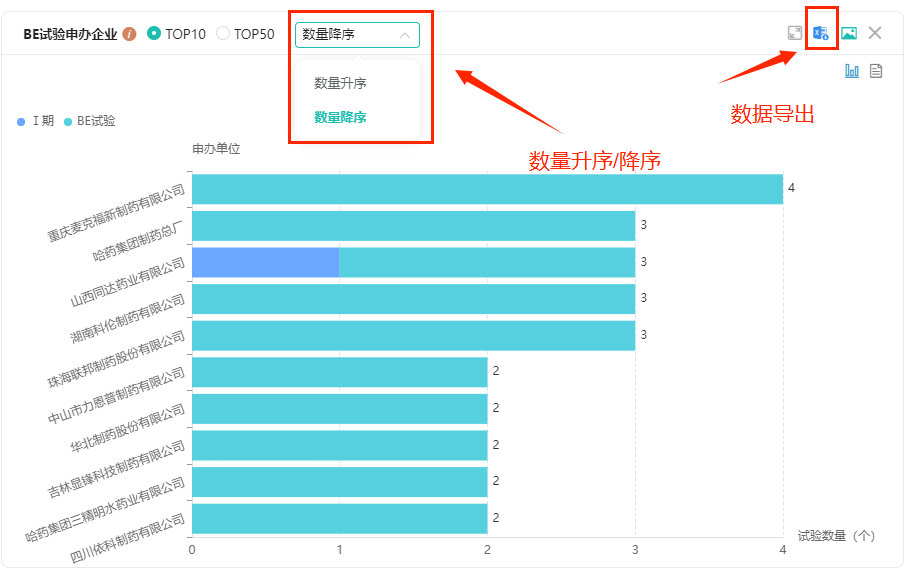
2. 查看百济神州2024年登记的国际多中心试验情况
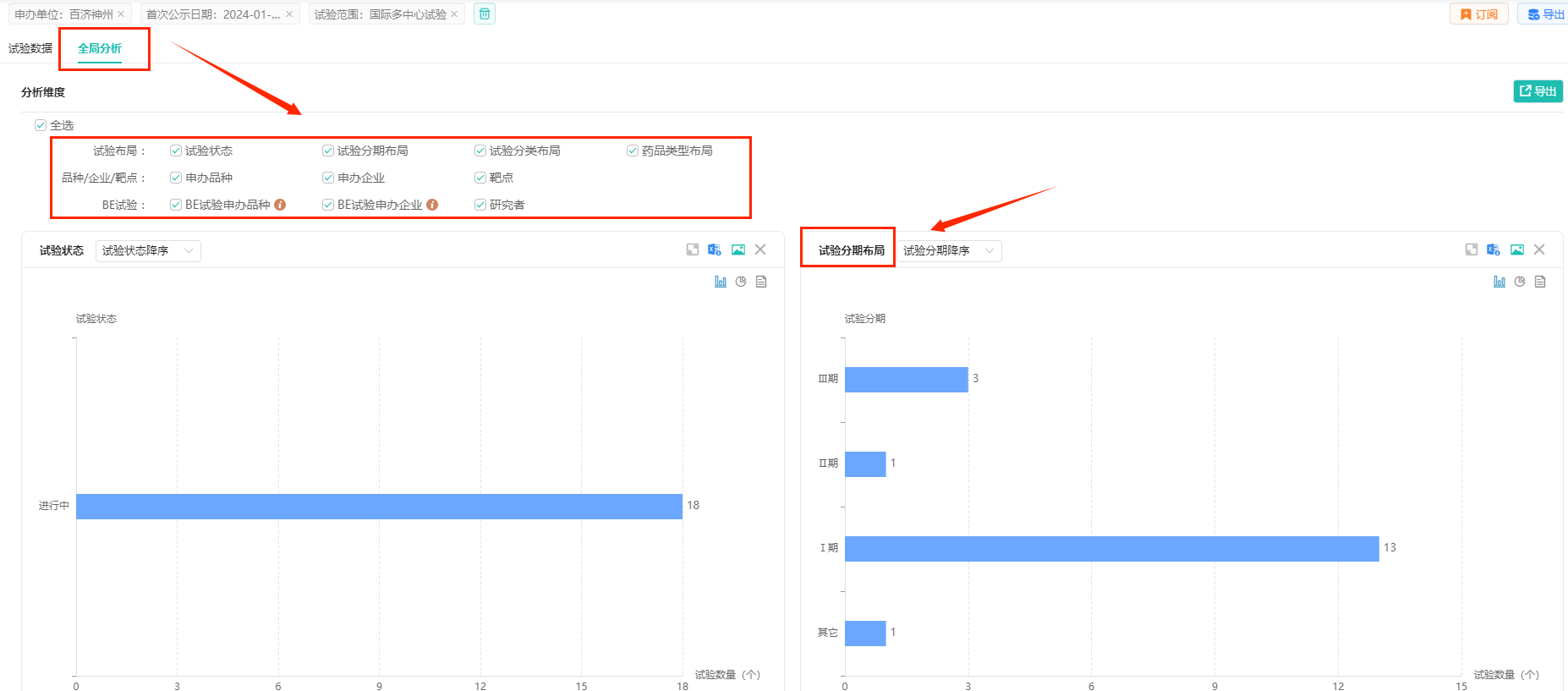
操作路径:【申办单位】输入【百济神州】,【首次公示日期】选择【2024年1月1日至2024年12月31日】,【试验范围】选择【国际多中心试验】,然后点击【搜索】按钮
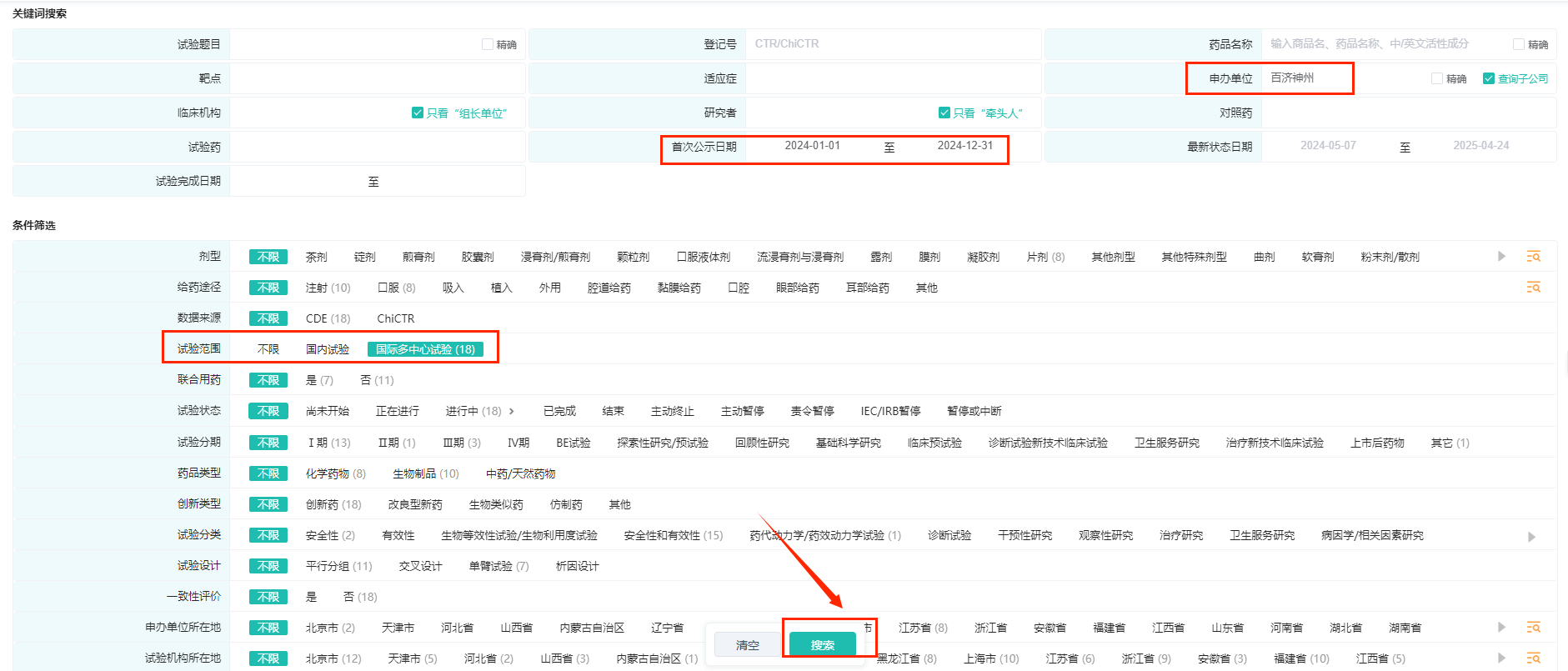
可以看到,百济神州在2024年登记的国际多中心试验,按登记号计有18个,涉及16个品种,有555家临床机构参与。
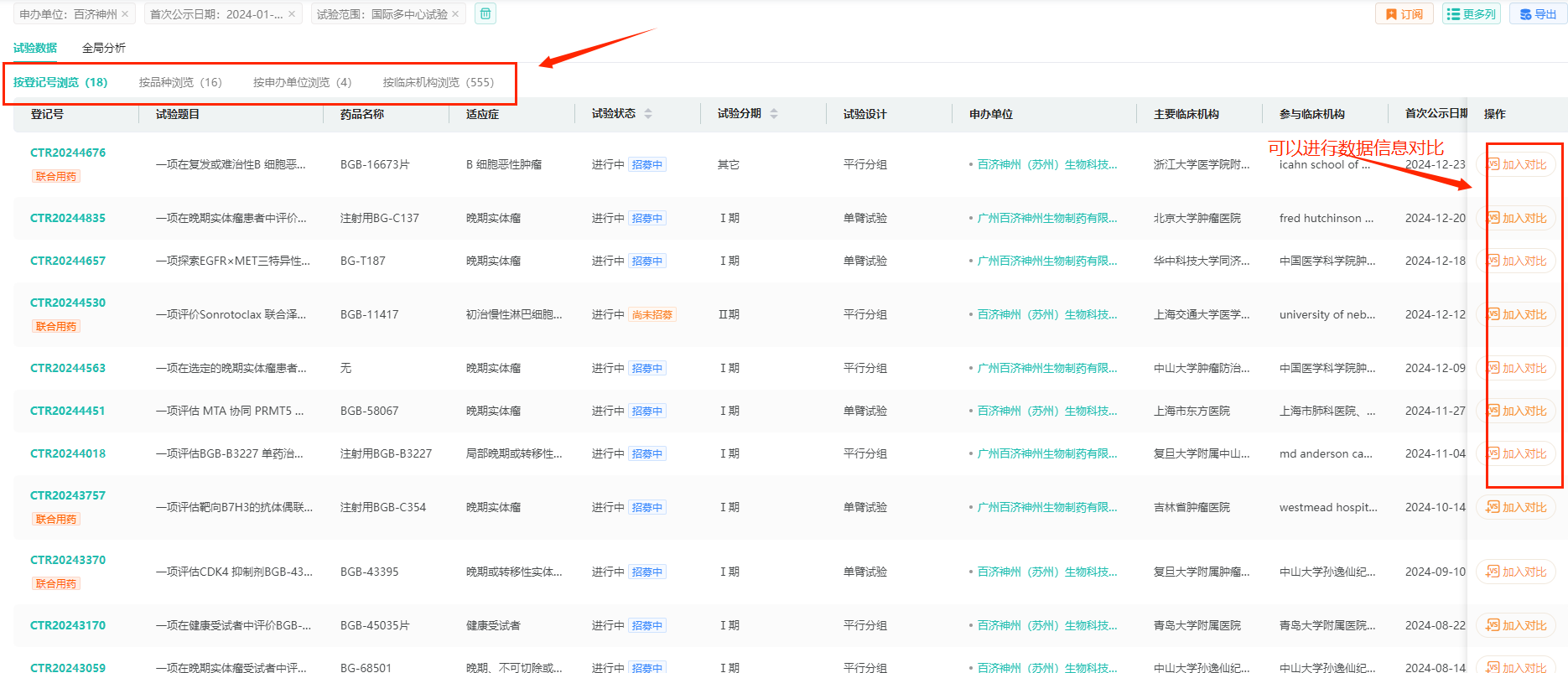
点击【全局分析】,可以看到试验状态、试验分期布局,试验分类布局,药品类型布局等数据信息;其中,2024年百济神州处于III期临床的有3个,II期临床3个,I期临床13个。
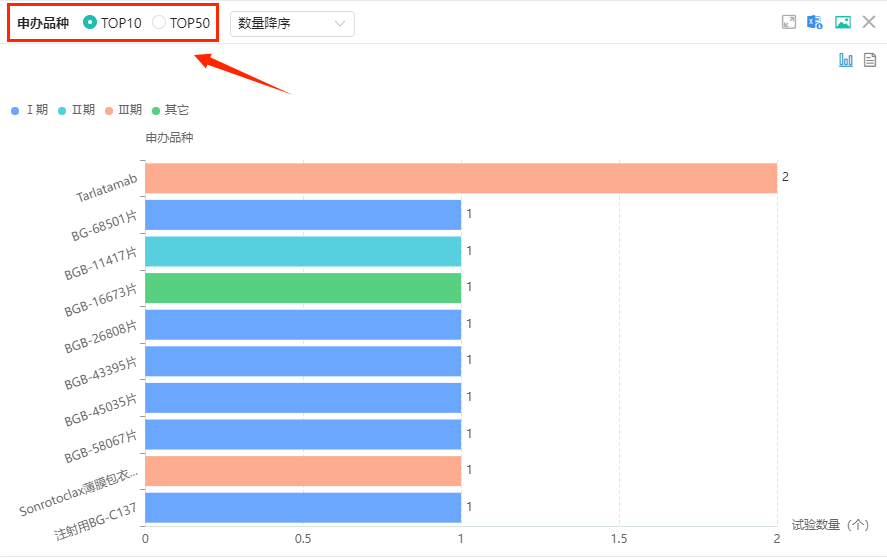
2024年百济神州临床试验热门申办品种TOP10分别有:Tarlatamab、BG-68501片、BGB-11417片、BGB-16673片、BGB-26808片、BGB-43395片、BGB-45035片、BGB-58067片、Sonrotoclax薄膜包衣片、注射用BG-C137。
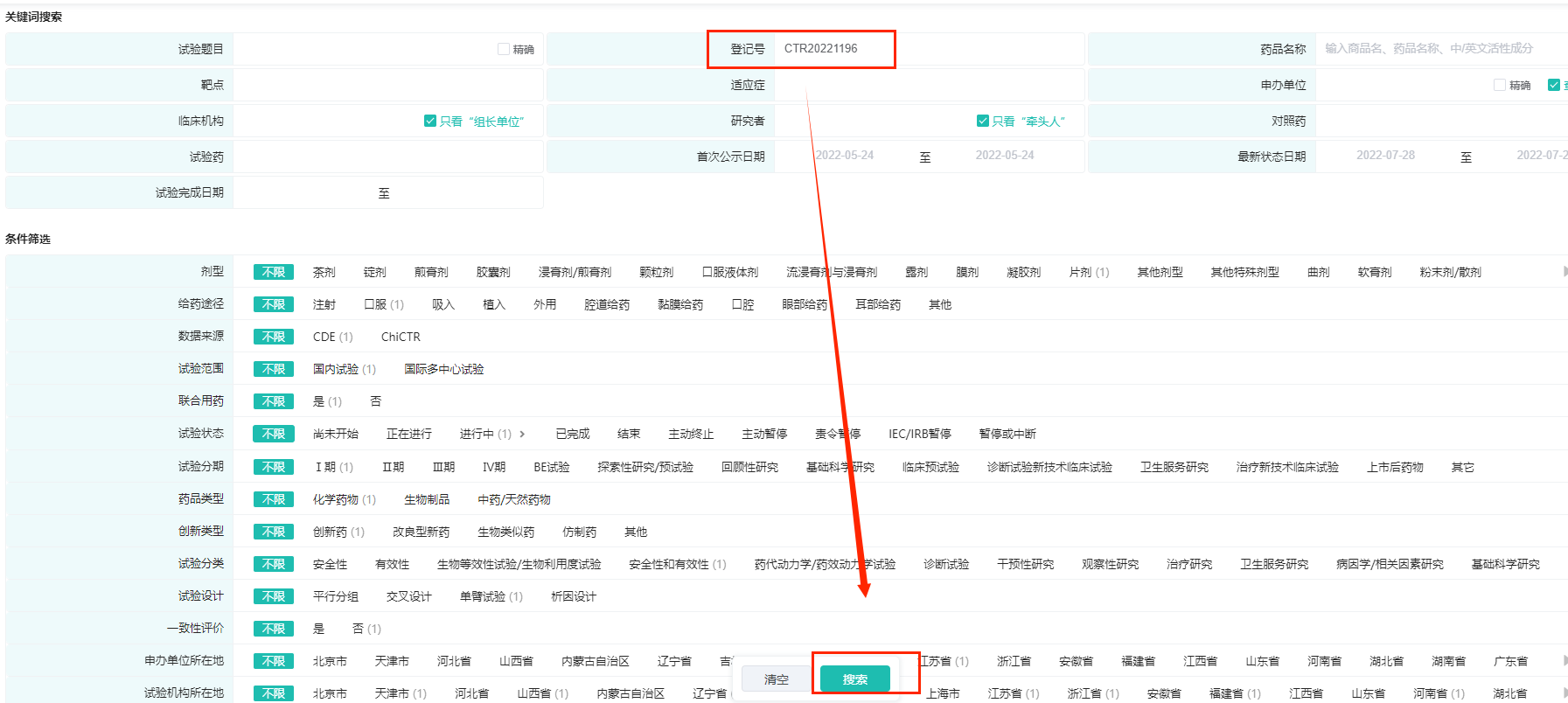
3. 查询登记号CTR20221196的临床试验详情
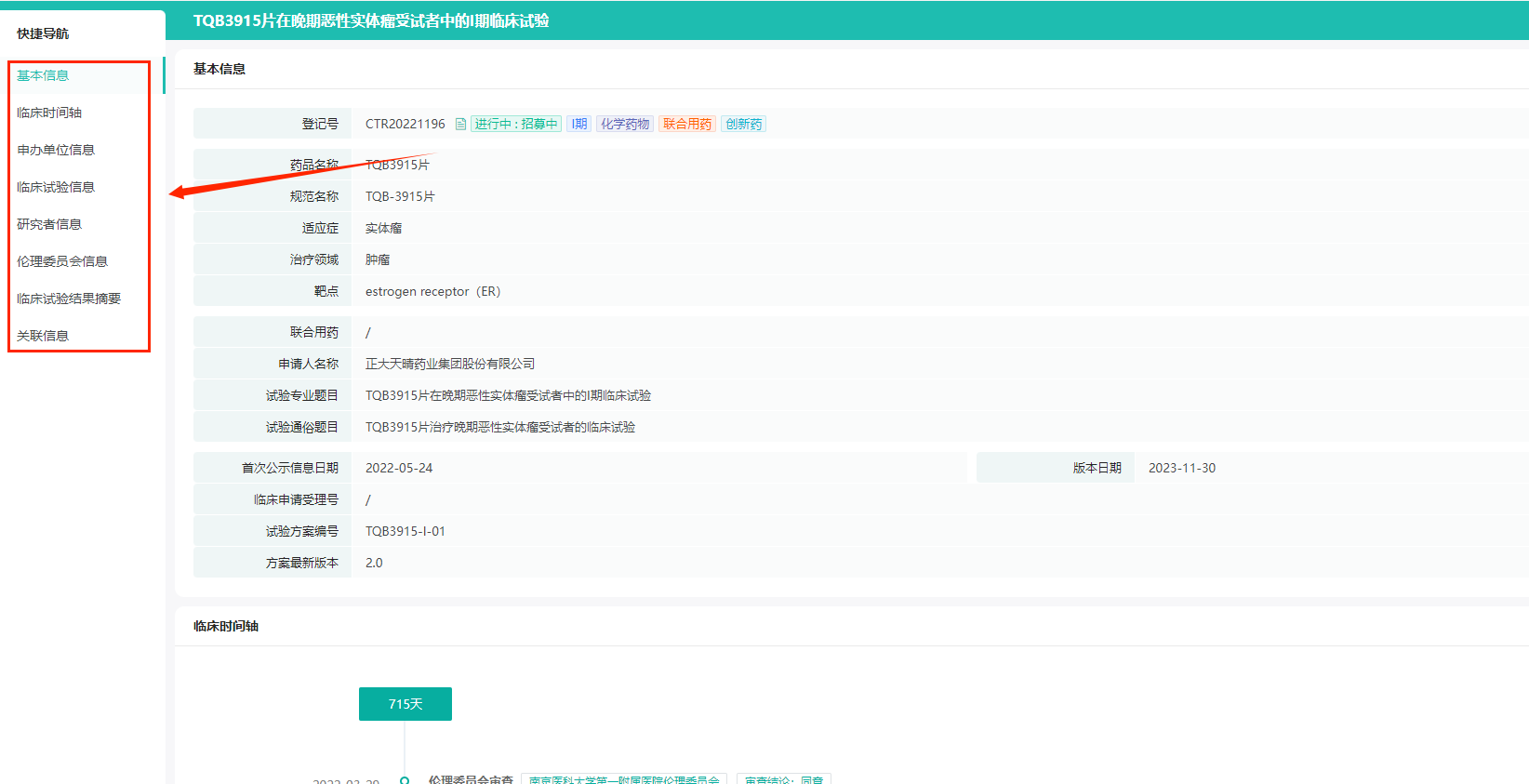
操作路径:【登记号】输入【CTR20221196】,然后点击【搜索】按钮,点击登记号可以查看CTR20221196的临床试验详情,如临床时间轴、申办单位信息,受试者信息、入选排除标准、试验药对照药、试验目的、参加机构等。
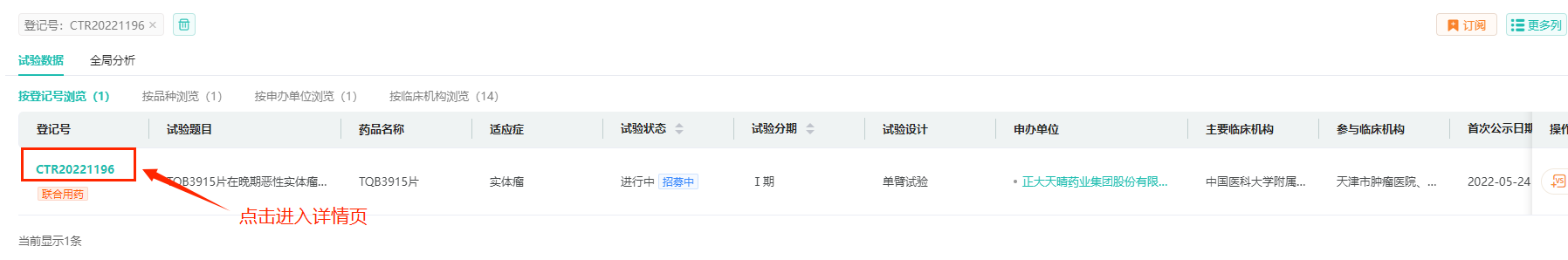
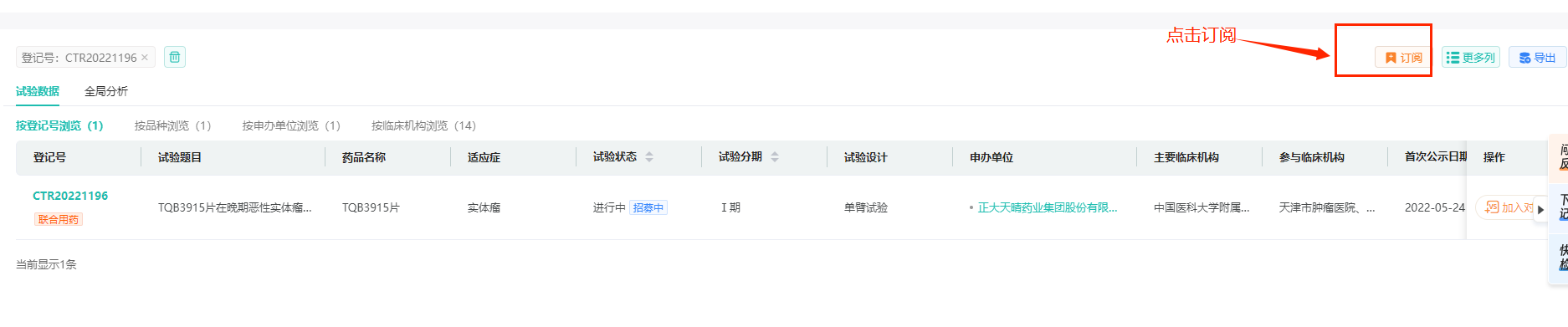
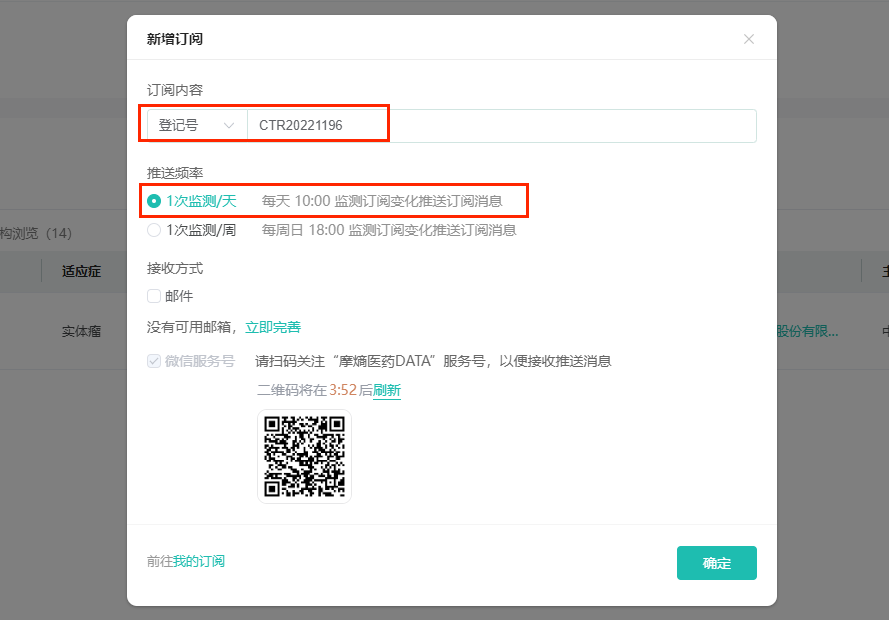
在查询结果页面,点击订阅,选择登记号,输入CTR20221196,选择推送频率1次监测/天或者1次监测/周,添加邮箱地址,就可以进行一键订阅,方便您更便捷实时地查看该临床试验最新动态,监测正大天晴TQB3915片的临床试验进度。
如上面解答未能解决您的问题,欢迎点击右侧【在线咨询】进行反馈。
四、联系我们
1. 关注【摩熵医药】公众号,实时获悉医药行业前沿资讯,全球医药情报一手掌握!
2. 申请试用中国临床试验数据库: https://vip.pharnexcloud.com/solution/clinical?auto=1
3. 数据库操作教程:https://vip.pharnexcloud.com/help/course
4. 数据库专题介绍:https://vip.pharnexcloud.com/solution/clinical